Ожирение и менопауза – важные индукторы полисоматических расстройств как по отдельности, так и в совокупности. Наличие ожирения в постменопаузе – отягощающий фактор, требующий особого внимания клинициста. Этому вопросу посвящена недавняя статья ведущих российских экспертов: профессора М. Р. Оразова, академика РАН В. Е. Радзинского, профессора А. И. Давыдова и соавт., опубликованная в журнале «Вопросы гинекологии, акушерства и перинатологии» [1].
Новаторские подходы к верификации ожирения
В настоящее время изменились диагностические подходы к верификации ожирения. Использование изолированного показателя индекса массы тела уже не представляется состоятельным, поскольку не отображает реальной картины [2]. Специалистам предлагается четкое разделение на доклиническую (без ассоциированных клинических состояний, рисков и осложнений) и клиническую (с ассоциированными клиническими состояниями и осложнениями) формы ожирения.
Изменение диагностических подходов привело и к эпидемиологическим сдвигам в оценке распространенности ожирения. Клиническое ожирение ассоциируется с повышением риска смертности в 2,7 раза [3]. Важно отметить, что ожирение более распространено среди женщин, причем распространенность напрямую коррелирует с возрастом [4].
Ожирение и постменопауза: временные параллели
Доказано, что избыточная масса тела и ожирение провоцируют развитие сердечно-сосудистых, онкологических заболеваний, психоэмоциональных нарушений, увеличивают вероятность гинекологической патологии [5]. У пациенток в пери- и постменопаузе вышеперечисленные риски кратно возрастают, к ним добавляется риск костно-мышечных нарушений и когнитивной дисфункции. При этом сама по себе менопауза может служить триггером для манифестации ожирения [4].
Ключевой особенностью женского организма является его зависимость от циклических гормональных изменений, которые со временем угасают (менопауза), и начинает развиваться системная гипоэстрогения. Поддержать эндокринно-метаболический статус помогает эстрадиол: он подавляет глюконеогенез и гликогенолиз в печени, усиливает выработку инсулина островками Лангерганса, значимо снижая уровень глюкозы крови и профилактируя инсулинорезистентность [6] (рис. 1).
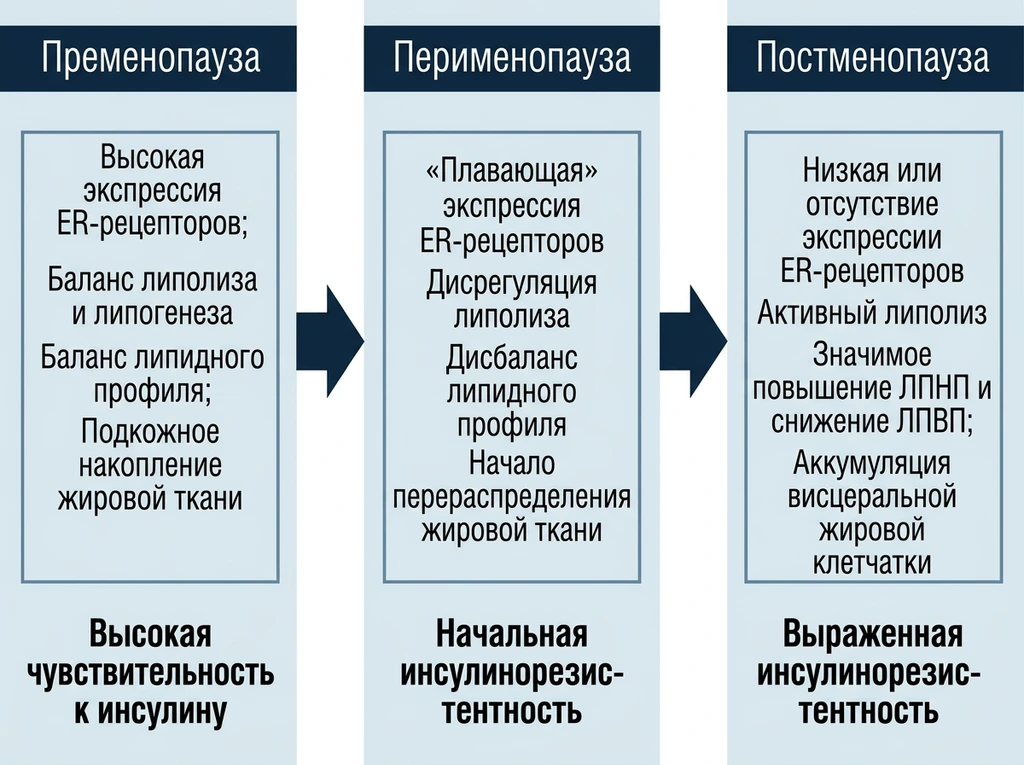
Рис. 1. Динамические изменения эндокринно-метаболического профиля в пери- и постменопаузе.
Клинические рекомендации по версии IMS
В декабре 2025 года вышли обновленные рекомендации IMS (Международное общество по менопаузе) по клиническому менеджменту женщин пери- и постменопаузального возраста [7]. Руководство содержит фундаментальные подходы к сохранению женского здоровья и профилактике полисистемных нарушений, индуцированных менопаузой. При отсутствии противопоказаний к менопаузальной гормональной терапии (МГТ) ее следует рассматривать как средство для купирования симптомов менопаузы. МГТ не рассматривается как средство для контроля массы или улучшения состава тела, однако может смягчить изменения в виде перераспределения жировой ткани в организме, снизить инсулинорезистентность и выраженность метаболических дисфункций.
МГТ является золотым стандартом лечения вазомоторного синдрома, остается терапией первой линии для профилактики потери костной массы, связанной с менопаузой, снижает риск развития сахарного диабета, а также ишемической болезни сердца у женщин до 60 лет, не имеющих сердечно-сосудистой патологии. Для пациенток с неконтролируемыми факторами риска сердечно-сосудистых заболеваний наиболее подходящим вариантом являются трансдермальные эстрогены из-за более низкого риска тромбоэмболических осложнений.
Преимущества трансдермальной доставки эстрогенов
Трансдермальные эстрогены вызывают меньше побочных эффектов, поскольку не метаболизируются в печени и не накапливают метаболиты с антиэстрогенной активностью. Они практически не влияют на липопротеины, глобулин, ферменты печени и факторы свертывания крови, а также снижают риск развития дислипидемии и образования камней в желчном пузыре [8]. В отличие от пероральных форм, трансдермальные препараты не повышают уровень тироксинсвязывающего глобулина. Риск венозных тромбоэмболий не увеличивается [9].
В исследовании III фазы с участием 454 женщин в постменопаузе установлено, что трансдермальный эстрадиола гемигидрат в форме спрея снижает частоту и интенсивность вазомоторных симптомов, практически не вызывает нежелательных реакций со стороны кожи и хорошо переносится [10,11].
Успешно зарекомендовал себя в клинической практике как удобное и эффективное средство для лечения менопаузальных расстройств трансдермальный спрей Лензетто®. Препарат был зарегистрирован в России. Он содержит раствор эстрадиола гемигидрата и октисалата в этаноле: 6,5 мл для 56 доз по 0,09 мл (1,53 мг эстрадиола на дозу). При нанесении на кожу образуется депо в роговом слое, обеспечивающее стабильную концентрацию эстрадиола в крови в течение 24 часов. Специальная насадка обеспечивает удобство нанесения и точность дозирования препарата (рис. 2).

Рисунок 2. Устройство для дозирования трансдермального спрея.
Заключение
Менопауза служит триггером для реализации ожирения, инсулинорезистентности и метаболических дисфункций, что необходимо учитывать при ведении пациенток. В основе рекомендаций IMS (2025) лежит научно доказанный риск-ориентированный подход. Одной из главных тенденций современной репродуктивной эндокринологии становится выбор трансдермального способа доставки эстрогенов как наиболее удобного и безопасного варианта МГТ, благодаря отсутствию первичного печеночного метаболизма.
Источники
- Оразов М.Р. и соавт. Менопауза и ожирение: реалии, риски и возможности преодоления. Вопросы гинекологии, акушерства и перинатологии. 2026, том 25, №1, с. 124–130
- Rubino F., Cummings D.E., Eckel R.H., Cohen R.V., Wilding J.P.H., Brown W.A. et al. Definition and diagnostic criteria of clinical obesity. Lancet Diabetes Endocrinol. 2025 Mar;13(3):221-262. DOI: 10.1016/S2213-8587(24)00316-4. Epub 2025 Jan 14. Erratum in: Lancet Diabetes Endocrinol. 2025 Mar;13(3):e6. DOI: 10.1016/S2213-8587(25)00006-3
- Fourman L.T., Awwad A., Gutierrez-Sacristan A., Dash C.A., Johnson J.E., Thistle A.K. et al. Implications of a New Obesity Definition Among the All of Us Cohort. JAMA Netw Open. 2025 Oct 1;8(10):e2537619. DOI: 10.1001/jamanetworkopen.2025.37619
- Чилова Р.А., Мартина М.Н., Сычев Д.А., Маслов С.С., Ляндау Ю.В., Неофиту Э.Г. и др. Ожирение и женская фертильность. Социально-экономические аспекты нарушения питания. Вопросы гинекологии, акушерства и перинатологии. 2024;23(3):66-77. DOI: 10.20953/1726-1678-2024-3-66-77
- Koufakis T., Patoulias D., Kaur K.K., Popovic D.S. Editorial: Weighing the impact of being overweight on female reproductive function and fertility. Front Reprod Health. 2025 Feb 3;7:1554284. DOI: 10.3389/frph.2025.1554284
- Patel P., Patil S., Kaur N. Estrogen and Metabolism: Navigating Hormonal Transitions from Perimenopause to Postmenopause. J Midlife Health. 2025 Jul-Sep;16(3):247-256. DOI: 10.4103/jmh.jmh_75_25
- Panay N., Fenton A., Hamoda H., Hillard T., Islam R., Pedder H. et al; (IMS Publication Steering Committee) and The IMS Recommendations Writing Group; IMS Recommendations Writing Group; With valuable support provided by. International Menopause Society (IMS) recommendations and key messages on women's midlife health and menopause. Climacteric. 2025 Dec;28(6):634-656. DOI: 10.1080/13697137.2025.2585487
- Kuhl H. Pharmacology of estrogens and progestogens: influence of different routes of administration. Climacteric. 2005;8 Suppl 1(sup1):3-63. DOI: 10.1080/13697130500148875
- Sobel T.H., Shen W. Transdermal estrogen therapy in menopausal women at increased risk for thrombotic events: a scoping review. Menopause. 2022;29(4):483-490. DOI: 10.1097/GME.0000000000001938
- Buster JE, Koltun WD, Pascual ML, Day WW, Peterson C. Low-dose estradiol spray to treat vasomotor symptoms: a randomized controlled trial. Obstet Gynecol. 2008 Jun;111(6):1343-51. DOI: 10.1097/AOG.0b013e318175d162
- Buster JE. Low-dose estradiol spray: a novel treatment for vasomotor instability in postmenopausal women. Womens Health (Lond). 2009 Jan;5(1):23-8. DOI: 10.2217/17455057.5.1.23



